自然界的一切物質都是由大量分子組成的,組成物質的分子間有一定的距離,分子間存在著相互作用力,這種作用力有時表現為引力,有時表現為斥力;同時,分子又處于無規則的永不停息的運動中,而這種大規模分子的雜亂無章運動稱之為熱運動。
由于分子間的作用力和分子熱運動等原因,使物質在通常狀態下呈現出三種不同的狀態,即固態、液態和氣態。
固態時,分子間的距離最近,相互間的引力最大。它把分子束縛在平衡位里附近,熱運動僅表現為在平衡位置附近的微小振動,而不能相對移動。因此,固態時的物質既有一定的體積,又有一定的形狀,并且還具有一定的機械強度。
液態時,分子間的距離仍較近,分子間的引力仍較大,足以使分子之間保持一定的距離。因此,液態物質有固定的體積,并能形成自由表面。另一方面液態物質的分子既可在平衡位置附近振動,又可單個的或成群的相對移動,所以說液態物質具有流動性而沒有一定的形狀。
氣態時,分子間距離大,而引力很小,甚至分子之間不能相互約束。因此,氣態物質既沒有一定的形狀,又沒有一定的體積,它可以充滿任何空間。組成物質的分子在熱運動中相互發生碰撞后又會發生旋轉運動。同時,組成分子的原子也進行著振動。
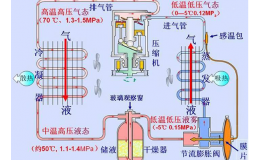
同一種物質在不同的條件下,由于分子間作用力和分子熱運動的結果,也會分別以不同的狀態存在。例如,標準大氣壓條件下,將水冷卻到0℃以下就會變成冰;而將水加熱到99.974℃以上就會變成水蒸氣。所以,物質的三種狀態盡管表現形式不同,但是在一定的條件下(即壓力和溫度變化到一定程度),物質的狀態就會發生變化。伴隨物質狀態變化過程的進行,一定有熱交換現象,如圖1.1.1所示。

物質由液態變成氣態的過程叫做汽化,汽化現象有兩種表現形式:一種是指在任何溫度下(只要低于臨界溫度)液態物質表面進行的逐漸汽化現象叫做蒸發;另一種是指在一定的條件下(沸點)液態物質的內部和表面同時進行的劇烈汽化現象叫做沸騰。需要注意的是:制冷技術中使用的“蒸發”概念,通常指的是沸騰。反之,物質由氣態變成液態的過程叫做液化,液化是汽化的逆過程。制冷技術中使用的“冷凝”概念,通常指的是液化。人為控制(或改變)某種物質所處的環境條件,就可以按照自己的意志迫使物質狀態發生變化,從而實現預期的目的。